Эмбрионы мышей без яйцеклеток и сперматозоидов: как такое возможно и что дальше?

Двум группам исследователей удалось вырастить эмбрионы из стволовых клеток, и они жили так долго, что ученым даже удалось рассмотреть формирование некоторых органов.
▶ Читайте также: Эмбрионы мышей, выращенные «в пробирках», образуют органы и конечности
Рецепт создания млекопитающего прост: возьмите яйцеклетку, добавьте сперматозоиды и ждите. Однако, согласно результатам двух новых работ, есть и иной путь. При подходящих условиях стволовые клетки способны делиться и самоорганизовываться в эмбрион. В ходе исследований, результаты которых опубликованы в Cell [1] и Nature [2] в августе 2022 года, двум группам ученых удалось вырастить эмбрионы мышей, а развитие самих организмов длилось дольше, чем в каких-либо предыдущих экспериментах. Рост эмбрионов продолжался в течение восьми с половиной дней, что было достаточным для развития отдельных органов — сердца, способного сокращаться, кишечной трубки и даже нервных валиков.
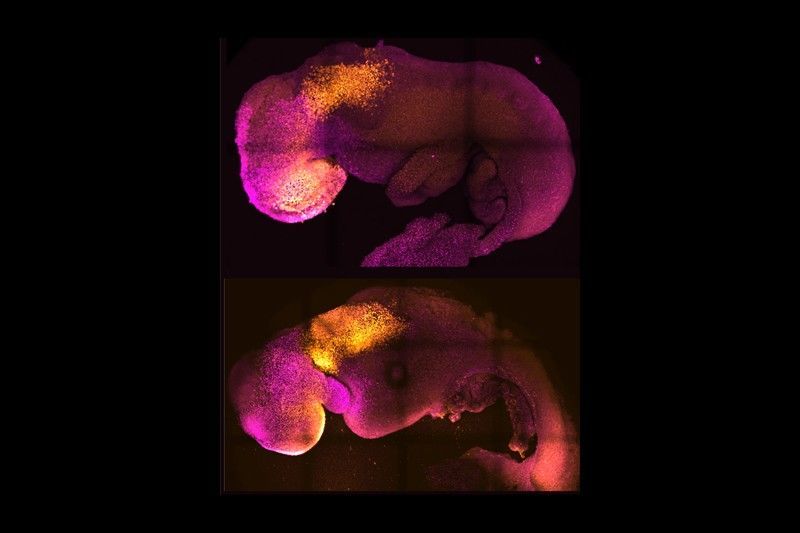
Рисунок 1 | Естественный и «искусственный» мышиные эмбрионы, выращенные эмбриологами под руководством Магдалены Зернцкой-Гетц
Процесс далек от совершенства. Только у небольшого процента клеток развиваются упомянутые особенности, и даже они не полностью имитируют естественное эмбриональное развитие. Однако работа по-прежнему представляет собой большой шаг вперед, который поможет ученым рассмотреть развитие органов с беспрецедентной детализацией. Как говорит Цзяньпин Фу, биоинженер из Мичиганского университета в Анн-Арборе, это очень, очень увлекательно. По его словам, следующей вехой в этой области, скорее всего, станет создание искусственного человеческого эмбриона на основе стволовых клеток.
Две группы исследователей достигли успеха, используя схожие методы. Магдалена Зерницка-Гетц, специалист по эмбриологии и стволовым клеткам, вместе с лабораториями Кембриджского университета (Великобритания) и Калифорнийского технологического института в Пасадене работает над этим вопросом в течение десяти лет. Она поясняет, что работа началась с эмбриональных стволовых клеток, которые могут служить моделью ранних этапов онтогенеза, однако прогресса в экспериментах не было. Затем, несколько лет назад, ее группа обнаружила [3], что при добавлении стволовых клеток, которые давали начало плаценте и желточному мешку, эмбрионы могли развиваться дальше. В прошлом году они продемонстрировали [4], что эту технику можно применить для выращивания эмбрионов до седьмого дня. В своей последней статье, опубликованной 25.08.2022 в Nature, команда Зерницкой-Гетц описывает выращивание эмбрионов в течение еще полутора суток.
Эмбрионы в пробирке
Команде Зерницкой-Гетц удалось осуществить это с помощью методики, разработанной Джейкобом Ханной, специалистом в области стволовых клеток из Института Вейцмана в Израиле, который также много лет работает над этим вопросом. В прошлом году команда Ханны сообщила о разработке аппарата [5], который позволил им выращивать естественные эмбрионы мышей вне матки в течение беспрецедентного периода времени. В этом инкубаторе, поддерживающем эмбрионы с пятого по одиннадцатый день, применены ранее разработанные технологии: эмбрионы находятся в стеклянных пузырьках, которые вращаются в системе, похожей на колесо обозрения; однако команда Ханны внесла новшество — вентиляцию. Система вентиляции контролирует состав смеси кислорода и углекислого газа, которая поступает в пузырьки, а также давление.
После того, как в прошлом году вышла статья Ханны, его команда поделилась некоторыми деталями своего инкубатора с другими эмбриологами и специалистами по стволовым клеткам. По словам Ханны, «мозгом» этого устройства команда предоставила всем, кто был в этом заинтересован, в том числе Зерницкой-Гетц и ее коллегам. А они уже немного доработали его для своих экспериментов. В статье, опубликованной в Cell 1 августа 2022 года, команда Ханны описывает, как они использовали эту систему для выращивания эмбрионов в течение восьми с половиной дней. Полный срок беременности у мышей составляет около 20 дней.

Рисунок 2 | «Искусственные» мышиные эмбрионы, выращенные внутри стеклянных пузырьков группой ученых под руководством специалиста по стволовым клеткам Джейкоба Ханны
Этого периода достаточно, чтобы развились области мозга, сердце начало сокращаться и сформировались нервные и кишечные трубки. Такие «искусственно» созданные эмбрионы очень напоминают естественные, образующиеся при оплодотворении яйцеклетки, однако, по словам Ханны, они не были стопроцентными копиями. Можно было обнаружить некоторые дефекты и изменения размеров формирующихся органов.
Каждая команда выращивала эмбрионы путем комбинации трех различных типов клеток. А команде Ханны удалось создать все три типа из наивных эмбриональных стволовых клеток. По словам ученого, это позволяет упростить процесс: начать его можно с одной клеточной популяции. Команда Зерницкой-Гетц сообщила об аналогичном достижении в препринте, опубликованном [6] на сайте bioRxiv (в своей статье в Nature исследователи использовали для создания эмбрионов линию клеток-предшественников из плаценты).
Развитие мозга
Команда Зерницкой-Гетц также провела эксперимент, в ходе которого ученые осуществили генетический нокаут гена Pax6, играющего ключевую роль в онтогенезе мозга. При удалении этого гена голова мыши развивалась неправильно, имитируя то, что происходит у естественных эмбрионов, у которых отсутствует этот ген. По словам Зерницкой-Гетц, этот результат показывает, что система действительно работает.
Как заявляет Мартин Пера, специалист по стволовым клеткам из Jackson Laboratory Center for Precision Genetics (Джексоновская Лаборатория точной генетики) в Бар-Харборе (штат Мэн), эти две статьи дополняют друг друга. Две очень профессиональные научные группы независимо получили поразительно схожие результаты.
Для исследователей эти искусственные модели имеют много преимуществ перед естественными эмбрионами, развивающимися вследствие оплодотворения. Так как они растут вне матки, за ними гораздо легче наблюдать. Также к ним значительно проще применять методики редактирования генома. По словам Фу, ученые могут проводить различные манипуляции и нокаут как мышиных, так и человеческих генов. Благодаря этому, такие модели могут оказаться полезны для определения роли различных генов в формировании врожденных дефектов или нарушений развития. Зерницка-Гетц планирует применять эту модель для выяснения причин прерывания беременностей.
Ханна надеется использовать эту методику для разработки искусственных эмбрионов человека, которые могут стать источником новых органов и тканей для нуждающихся в них людей.
А что насчет людей?
Однако добиться переложения экспериментально полученных результатов на человека будет крайне непросто. Исследователи добились превращения человеческих стволовых клеток в бластоцисты и даже имитации ими некоторых аспектов гаструляции (этапа онтогенеза, когда происходит формирование зародышевых листков эмбриона, состоящих из разных типов клеток). Однако достижение стадии формирования органов из клеток человека, наступающей примерно через месяц после оплодотворения, является серьезной технической проблемой. Тем не менее, Али Бриванлоу, эмбриолог из Рокфеллеровского университета в Нью-Йорке, настроен оптимистично. По его мнению, цели вполне ясны.
Другой аспект — этические проблемы, возникающие на более поздних стадиях развития эмбриона. Один из ключевых спорных вопросов заключается в том, следует ли считать такие искусственно созданные структуры эмбрионами. Международное общество по исследованию стволовых клеток уже долгое время не рекомендует культивировать человеческие эмбрионы после 14-го дня (что эквивалентно 6-му дню у мыши) — примерно в это время появляется первичная полоска (структура, знаменующая начало гаструляции). В 2021 году Общество сняло ограничение и выпустило руководство, согласно которому такие исследования должны иметь убедительное научное обоснование и использовать минимальное количество эмбрионов, необходимых для достижения научной цели.
Тем не менее, Пера видит необходимость в продолжении разговора о биоэтике применения таких моделей. В течение многих лет исследователи работали с моделями человеческих эмбрионов без особого сопротивления со стороны правозащитников. Однако Пера беспокоится о той негативной реакции, которая неминуемо возникнет, поскольку у ученых появляется возможность разрабатывать модели человеческих эмбрионов, у которых уже формируются органы. Он считает, что такая реакция может поставить под угрозу всю область исследований. Как добавляет Пера, важно, чтобы люди знали, что предлагается в ходе исследований, а сами эксперименты проводились бы на основе некоего этического консенсуса. Теперь каждый шаг должен совершаться с осторожностью.
