Имплантация электрода в область передней поясной извилины для лечения алкоголизма

Алкогольная зависимость довольно часто сочетается с другими психическими расстройствами, например, тревожными (27,6 %), расстройствами настроения (23,5 %) и личности (39.5 %), и в таких ситуациях особенно тяжело поддается лечению. А одна из основных проблем терапии алкогольной зависимости — «срывы»: 85 % пациентов рано или поздно возвращается к употреблению алкоголя. Выделяют три основных причины таких срывов: непреодолимое влечение к алкоголю, напоминания об алкоголе во время воздержания и стрессовые ситуации. Занявшись лечением всерьез, последние два фактора можно исключить, а на первый — воздействовать современными методами терапии.
Например, влечение к алкоголю можно подавить путем периодической транскраниальной магнитной стимуляции (пТМС) дорсолатеральной префронтальной коры. При этом повышается высвобождение дофамина в прилежащем ядре (nucleus accumbens) и хвостатом ядре (nucleus caudatus), а также модулируется высвобождение дофамина в передней поясной извилине и орбитофронтальной коре. Однако эффект такой терапии непродолжителен, особенно если учитывать возможную генетическую предрасположенность к алкоголизму, связанную с изменениями в дофаминовых рецепторах 2 и 3 типов. А вот если обеспечить постоянную стимуляцию истощаемой дофаминовой системы, есть шанс добиться стойкого эффекта.
О пациенте
Мужчина 38 лет, в анамнезе не поддающаяся лечению алкогольная зависимость, а также коморбидное тревожное расстройство и агорафобия. До становления алкогольной зависимости пациент употреблял амфетамины и чрезмерно увлекался азартными играми. Принимать алкоголь начал в возрасте 17 лет, чтобы справиться с паническими атаками, по большей части связанными с агорафобией: например, выпивал перед выходом из дома, чтобы подавить тревогу. Постепенно алкоголь стал основным предметом его забот, пациент всегда следил, есть ли дома что-нибудь выпить, на случай, если ему вдруг понадобится спиртное, но от окружающих свою привычку скрывал.
Пытался сам контролировать употребление алкоголя и время от времени задавал себе ограничение: выпивал в день не более 4 банок пива с самым высоким содержанием алкоголя, которое смог найти (10 градусов, в одной банке 500 мл). Когда понял, что самостоятельно справиться с зависимостью не может, обратился сначала в общество Анонимных Алкоголиков, затем консультировался у психолога и лечился у нарколога. Пробовал медитацию, практику осознанности, 10 раз ему подшивали имплант с дисульфирамом (антабусом). Поначалу антабус помогал, но как только имплант извлекали, начинал пить еще больше, чем раньше, в том числе с эпизодами компульсивного потребления алкоголя до потери сознания, когда, очнувшись, он опять начинал пить. Поскольку амбулаторное лечение не помогало, пациент несколько раз госпитализировался в психиатрический стационар, там лечение снова давало эффект, но снова ненадолго. В бельгийскую клинику, где занимаются лечением алкоголизма методами нейромодуляции, он обратился после того как увидел в средствах массовой информации сообщение об успешном лечении алкоголизма с помощью пТМС. На момент обращения он оценил влечение к алкоголю на 9,5 по шкале от 0 — отсутствие влечения до 10 — максимально возможное влечение.
В центре провели следующие исследования:
1) Функциональная магнитно-резонансная томография (фМРТ) для визуализации областей, «ответственных» за влечение к алкоголю; оценивалась их активация (а именно гемодинамическая ответная реакция зависимости уровня кислорода в крови — BOLD) в ответ на изображения, связанные и не связанные с ситуациями употребления спиртного. Таким образом предварительно локализовали «источник» патологической активности, ассоциирующийся с влечением к алкоголю.
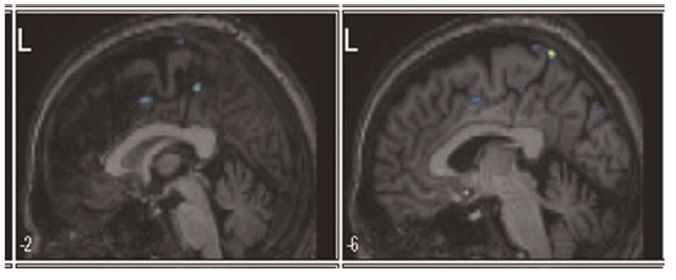
Рисунок 1. На фМРТ в сагиттальной проекции видны участки BOLD-активации в дорсальной части передней поясной извилины/дополнительной моторной области (участок кпереди) и левого предклинья (участок кзади) за месяц до хирургической операции.
2) Результаты фМРТ подтвердили методом электроэнцефалографии совместно со стандартизированной электромагнитной томографией низкого разрешения (sLORETA). Этот метод позволяет обнаружить источник электрической активности, которая при ЭЭГ регистрируется с поверхности черепа. В отличие от фМРТ, это исследование проводится без всякой стимуляции, с закрытыми глазами, все внешние стимулы и артефакты исключаются. Данные пациента сравнили с результатами 15 здоровых мужчин, подобранных по возрасту.

Рисунок 2. ЭЭГ с sLORETA в покое в сравнении с контрольной группой по бета-ритму (12-30 Гц) выявила повышенную спонтанную активность в области передней поясной извилины/дополнительной моторной области с распространением на фронтополярную кору (поле 10 по Бродману) — левое верхнее и правое нижнее изображение, за месяц до хирургической операции.
Лечение
Начать терапию решили с неинвазивной нейромодуляции путем пТМС двойным коническим индуктором, чтобы спрогнозировать, насколько этому пациенту будет полезна имплантация стимулятора.
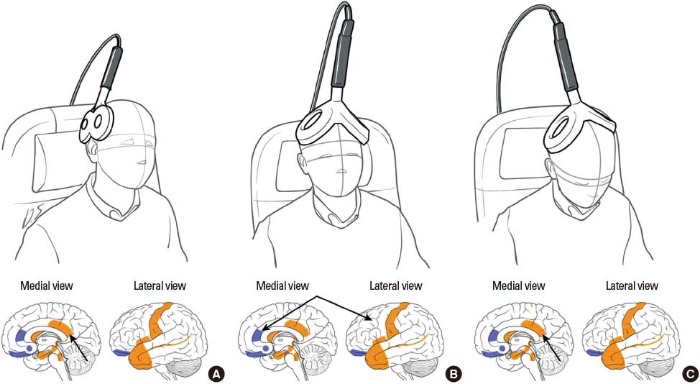
Стимуляция была направлена на область BOLD-активации по данным фМРТ и источник спонтанной активности по данным ЭЭГ-LORETA. Через две недели состояние пациента изменилось кардинально: силу влечения к алкоголю он оценил на 2 балла из 10 (по сравнению с первоначальными 9,5). Но, как ранее говорилось, через 6 недель эффект угас. Пациенту предложили плацебо-сессию, чтобы ни у кого не осталось сомнений в эффективности именно стимуляции, но пациент был так впечатлен результатами ТМС, что отказался от всех проверок и попросил сразу установить стимулятор.
Ход операции
После получения информированного согласия было проведено оперативное вмешательство: малая трепанация в правой лобной области и доступом через серп мозга введение двух электродов для билатеральной стимуляции дорсальной части передней поясной извилины. Нейронавигация осуществлялась с помощью безрамной системы Stealth.

Разрез кожи проводили в лобной области по линии роста волос, пересекая срединную линию. Трепанационное отверстие размером 4х4 см было выполнено прямо над верхним сагиттальным синусом. Твердую мозговую оболочку рассекли U-образным разрезом, обнажив серп мозга, чтобы провести устройство для нейронавигации между правой лобной долей и серпом.
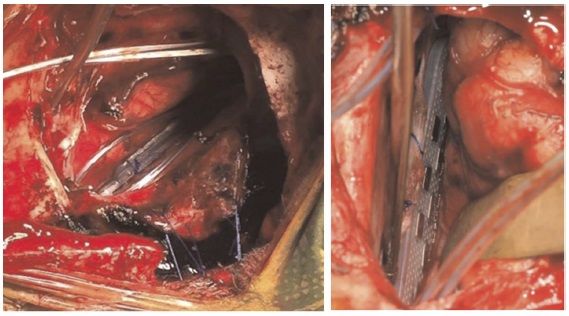
Когда целевой участок был локализован, серп рассекли и поместили электроды — Lamitrode 44, американского производства — свободно в области мозолистого тела, латеральнее околомозолистых артерий. Их соединили задними поверхностями и поместили в области, определенные при фМРТ, так, чтобы они располагалась непосредственно под серединой электродов, чтобы компенсировать возможные погрешности в навигации и интраоперационные смещения.
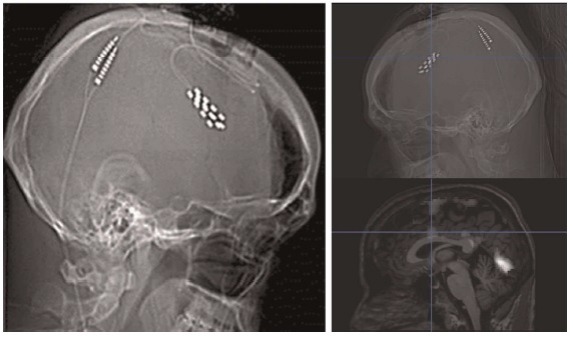
Затем электроды дополнительно подшили к серпу, чтобы предотвратить послеоперационные смещения. После промывания операционной области твердую мозговую оболочку зашили и трепанационное отверстие закрыли с использованием системы Craniofix.
Электроды под кожей провели к теменной области, там присоединили к удлинителю далее вывели на переднюю поверхность грудной клетки, где через второй удлинитель вывели к правой стороне живота и подсоединили к генератору, который будет располагаться в этой области в кожном кармане.

На второй день после операции, когда в очередной раз у пациента появилась тяга к спиртному, электроды активировали, силу тока при стимуляции подобрали так, чтобы появился отчетливый эффект. Коррекции по побочным эффектам не потребовалось, поскольку их просто не было, в том числе симптомов абстиненции, которых врачи ожидали. На пятый день после операции пациент был выписан; влечение к алкоголю на тот момент он оценивал на 4 из 10. На приеме через 1, 3 и 6 месяцев после операции пациент утверждал, что оно снизилось до 1 из 10, вместе с тем исчезли тревожность и симптомы агорафобии.
По словам пациента, теперь он чувствовал себя «внутренне свободным», «будто камень с души свалился». Теперь он мог спокойно отправиться за покупками в торговый центр, где всегда многолюдно. Тяга к алкоголю полностью пропала, и из алкогольного отдела пациент теперь выходил с пустой тележкой, совершенно не испытывая потребности что-то купить. Освободившееся время он мог проводить с женой и дочерью. Через год пациент также бросил курить; симптомы зависимости, агорафобии и тревожности все еще отсутствовали через 18 месяцев после операции.
Вновь выполненная ЭЭГ с LORETA показала, что при выключенных электродах патологические альфа-осцилляции в передней поясной извилине все еще сохранялись, а обычная альфа-активность была по сравнению с результатами до операции, нормальной. Когда после 18 месяцев работы электроды отключили, все аспекты электрической активности в области интереса, кроме дельта-активности, пришли в норму.
Обоснование метода
Алкоголизм и ранее пытались лечить нейрохирургическими методами, например, с помощью цингулотомии и разрушения прилежащего ядра. Эффект был получен очень хороший, но были и нежелательные последствия (снижение устойчивости внимания после цингулотомии), к тому же у обеих операций есть серьезный недостаток: наносимое повреждение необратимо. Затем была предложена глубокая стимуляция прилежащего ядра, она оказалась эффективна у 3 пациентов из 6, перенесших эту процедуру, причем у одного из них была та же клиническая картина, что и у нынешнего пациента: зависимость, агорафобия и тревожность. Стимуляция именно передней поясной извилины с целью избавить пациента от зависимости ранее не проводилась и описывается впервые.
Однако в лечении других заболеваний имплантация электродов в эту область уже применялась, а именно при хронической боли и при эпилепсии, на этот опыт и опирались исследователи. Паттерн стимуляции, который применялся в этом случае, ранее был исследован на животных; он подбирался так, чтобы имитировать залповую активность нейронов, но при этом навязывать необходимый постсинаптический потенциал (возбуждения или торможения). Наибольший тормозный потенциал получали с помощью спайков с частотой 500 Гц, именно этот режим и взяли за основу стимуляции для данного пациента.
Недостаток этого случая, во-первых, в отсутствии плацебо-контроля, однако маловероятно, что эффект плацебо дал бы такое стойкое улучшение у пациента с такими тяжелыми симптомами; а во-вторых, в невозможности судить, насколько этот метод подойдет пациентам, не страдающим тревожностью и агорафобией, которые в какой-то степени послужили причиной зависимости в данном случае.
Источник: De Ridder D. et al. Anterior cingulate implant for alcohol dependence: case report //Neurosurgery. – 2016. – Т. 78. – №. 6. – С. E883-E893.
