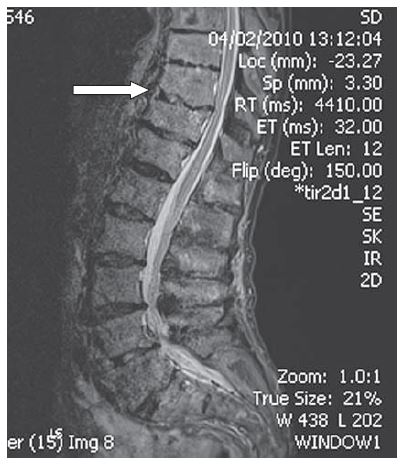
Болезнь Педжета
73-летний мужчина предоставляет вашему вниманию пятилетнюю историю развития боли в пояснице, которая с каждым годом становится интенсивнее. В течение прошлого года у него дополнительно появилась боль в области ягодиц и голеней. Купирование болевых ощущений парацетамолом не приносит облегчения. Неврологическое обследование ничем не примечательно. Рентгенограммы позвоночника показывают увеличение трабекулярного узора в нескольких поясничных и нижних грудных позвонках и расширение нескольких поясничных тел позвонков. Общий уровень щелочной фосфатазы в сыворотке составляет 350 U на литр (контрольный диапазон от 40 до 125); Результаты тестов функции печени и других обычных лабораторных тестов являются нормальными.
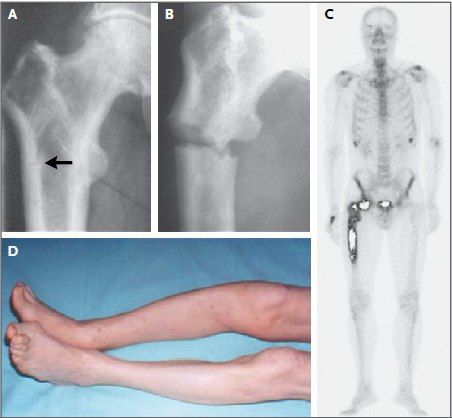
Болезнь Педжета впервые описана в 1876 британским хирургом и патологоанатомом Джеймсом Педжетом. Это заболевание, характеризующееся очагами повышенной костной резорбции и последующим формированием нарушенной архитектоники костей с пониженной биомеханической прочностью.
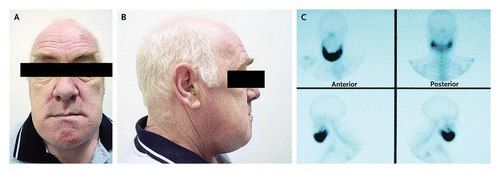
Эпидемиология
Редко встречается у лиц младше 50 лет, с возрастом частота увеличивается и поражает 5,8% женщин и 6,9% мужчин в возрасте старше 85 лет. Общая распространенность болезни среди лиц старше 55 лет составляет около 2%. У мужчин встречается в 1,6 раз чаще, чем у женщин. Заболевание распространено в северо-западных и южных регионах Европы и редко диагностируется у населения Скандинавских стран и Азии.
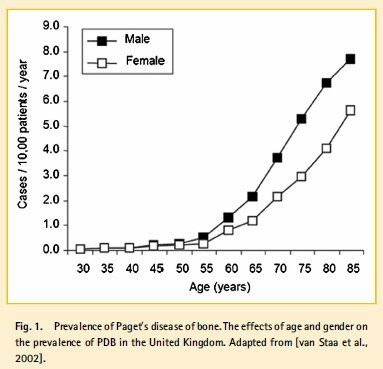
Факторы риска
- Повторные травмы костей
- Мутации в генах (см. таблицу) и отягощенный семейный анамнез с аутосомно-доминантным типом наследования. От 40 до 50% пациентов с семейной историей и от 5 до 10% пациентов со спорадическим заболеванием носят мутации в SQSTM1, который кодирует р62 белок, играющий ключевую роль в регуляции функции остеокластов.
- Синдром, включающий миопатию, болезнь Педжета и лобно-височную деменцию (Inclusion body myopathy associated with Paget disease of bone (PDB) and/or frontotemporal dementia (IBMPFD)); мутации в гене VCP на 9 хромосоме
- Токсины, содержащие мышьяк, свинец
- Длительный контакт с домашними и сельско-хозяйственными животными (противоречивые данные)
- Вирус кори (противоречивые данные). В Италии и Испании вакцина появилась только в 1976 и 1978 годах, что могло бы объяснить, почему заболеваемость болезнью Педжета в этих странах, по-видимому, не уменьшилась в той же степени, как и в других странах, которые раньше начали введение вакцин.
- Вирус собачьей чумы (противоречивые данные)
- Респираторно-синцитиальный вирус (противоречивые данные)

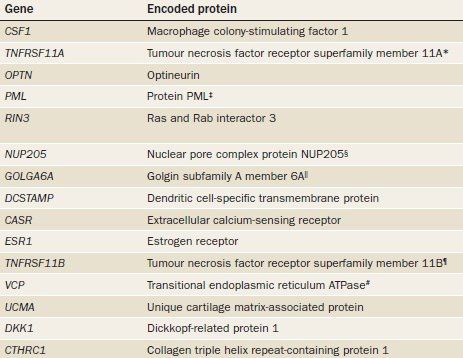
В течение жизни нормально функционирующая кость постоянно обновляется. При формировании костной ткани остеобласты попадают в костный матрикс и дифференцируются в остеоциты, которые, как считается, действуют как сенсоры и играют важную роль в регуляции активности остеобластов и остеокластов путем продуцирования рецепторного активатора Nuclear Factor Kappa B Ligand (RANKL) и склеростина. При болезни Педжета нарушается работа остеокласт-остеобластной связи, что приводит к аномалии микроструктуры кости. Было подсчитано, что скорость костной резорбции при БП увеличивается в 7 раз по сравнению с нормальной костью. Связано это с повышением количества и размеров остеокластов. Характерным признаком остеокластов при БП является наличие особых ядерных включений. Первоначально эти структуры считались парамиксовирусами, но позже предположили, что это агрегаты незараженных белков из-за дефектов в пути аутофагии.
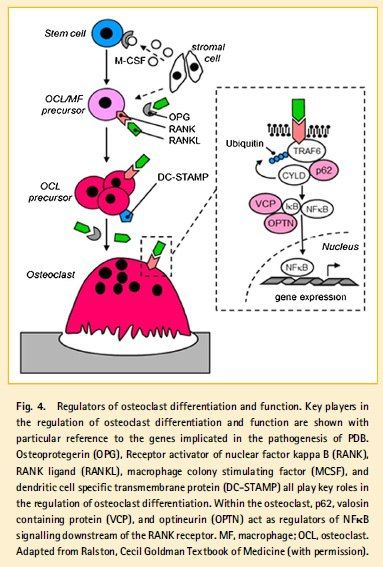
Резорбцию затем сменяет повышенное образование новой костной ткани. Однако, хаотичный способ её закладки приводит к нарушению архитектоники и понижению механической прочности кости. В процессе формирования новой костной ткани значительно повышается её васкуляризация. В дополнение к этому, развивается фиброз костного мозга.
Аномалия аутофагии объясняется тем, что многие из белков, вовлечённые в патогенез болезни Педжета, также участвуют в процессах аутофагии. Например, p62 играет важную роль в аутофагии, рекрутируя убиквитинированные белки в аутофагосому, взаимодействуя с белком легкой цепи (LC3). Было показано, что уровни LC3 и p62 увеличиваются в предшественниках остеокластов у мышей с мутацией P394L (эквивалент человеческой мутации P392L) . Также клинические исследования показали, что уровни p62 увеличены в B-клетках у пациентов с болезнью Педжета.
Помимо этого белок оптиневрин, который известен как медиатор болезни Педжета, связанный с локусом 10p13, играет роль в аутофагии. Наконец, Валозин-содержащий белок (VCP), который играет роль в патогенезе синдрома, включающего миопатию тела, болезнь Педжета и лобно-височную деменцию, также играет роль в аутофагии.
Хотя все данные указывают на дисрегуляцию пути аутофагии при болезни Педжета, в настоящее время остается неясным, связаны ли дефекты аутофагии с повышенным остеокластогенезом или является ли это побочным эффектом из-за участия белков, таких как p62, OPTN и VCP, которые сами играют роль в аутофагии.
Было проведено большое количество исследований для выявления возможных медиаторов и механизмов, которые лежат в основе повышенной активности остеокластов, характерной для болезни Педжета. Было установлено, что образцы костного мозга у пациентов с данной болезнью проявляют повышенную чувствительность к эффектам кальцитриола и RANKL по сравнению с контрольными культурами, что приводило к увеличению количества и размера генерируемых остеокластов.
Это указывает на то, что предшественники остеокластов у пациентов с болезнью Педжета оказываются гиперчувствительными к агентам, которые способствуют дифференцировке остеокластов и резорбции кости. Имеются данные о том, что эта гиперчувствительность обусловлена внутренними генетическим аномалиями в остеокластах и/или их предшественниках, помимо этого увеличивается производство остеокластогенных цитокинов костным мозгом.
Если говорить кратко, то патогенез можно условно разделить на 4 стадии:
- Повышенная костная резорбция (зачастую манифестирует в местах прикрепления мышц к костям)
- Фиброз костного мозга
- Повышенная васкуляризация кости (затрудняет проведение оперативных вмешательств, усугубляет СН у пожилых пациентов)
- Повышение активности остеобластов
- Формирование деформированной кости с нарушенной архитектоникой
Диагностика
Диагностика основывается на данных клинической картины, биохимического исследования крови и лучевых методов.
При решении вопроса о том, нуждается ли пациент в лечении, принято идентифицировать затронутые кости и сдавать анализы крови для оценки метаболической активности.
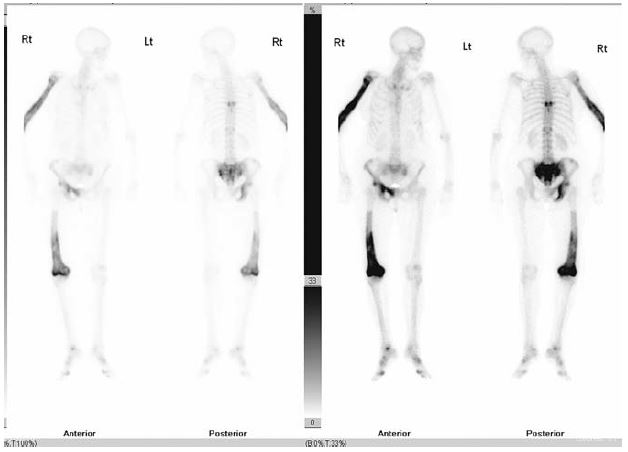
Рекомендованным исследованием для выявления пораженных костей является радионуклидное сканирование костей. Затем проводится рентгенологическое исследование всех пораженных костей.
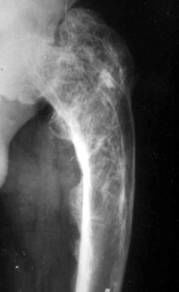
Затем анализы крови проводятся для измерения общей активности щелочной фосфатазы. Хотя ЩФ может быть получена из других органов (печень, почки, плацента) высокий уровень ЩФ в присутствии костного радионуклидного сканирования и рентгенологическое исследование обычно указывает на то, что заболевание является метаболически активным.
Если у вас есть какие-либо сомнения, например, у пациентов с сопутствующим заболеванием печени, можно измерить специфическую ЩФ костей, которая повышается в активной стадии болезни Педжета. Такие тесты на специализированные маркеры, как специфическая костная щелочная фосфатаза или проколлаген I типа, могут быть полезны у пациентов с сосуществующим заболеванием печени, но в противном случае они не имеют большого преимущества перед измерением общего уровня щелочной фосфатазы в сыворотке крови с целью диагностики и оценки ответа на лечение.
Если затронута только одна кость, то уровень ЩФ может сохраняться на нормальных значениях.
Помимо определения уровня щелочной фосфатазы рекомендуется оценка почечной функции, уровня кальция в крови, альбумина, 25-гидроксивитамина D. Функции печени следует оценивать, чтобы исключить возможность повышения уровня ЩФ из-за поражения печени.
Клиническая картина болезни Педжета очень разнообразна. У одних пациентов заболевание протекает бессимптомно, а у других развивается целый комплекс симптомов: боль в костях, их деформация, появление патологических переломов и развитие глухоты (из-за остеосклероза височной кости). В недавнем систематическом обзоре боль в костях была наиболее распространенной жалобой, возникающей примерно в 40% случаев, за которой следуют деформация (20%), патологический перелом (10%) и глухота (6%).
Наиболее распространенным симптомом является боль в костях, которая может быть вызвана увеличением костного кровообращения или осложнениями: остеоартрит, спинальный стеноз или псевдоперелом.
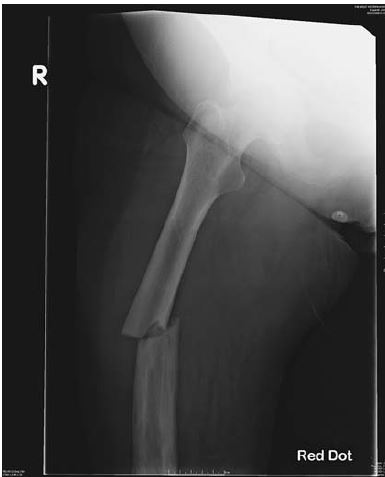
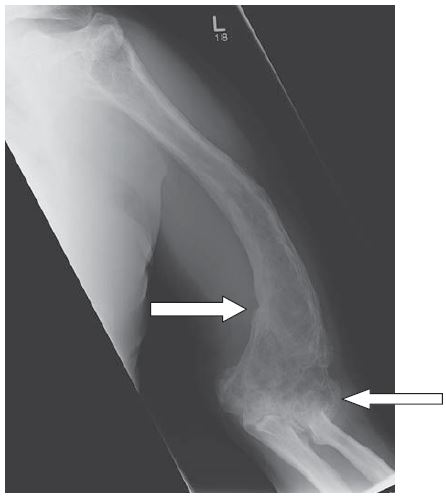
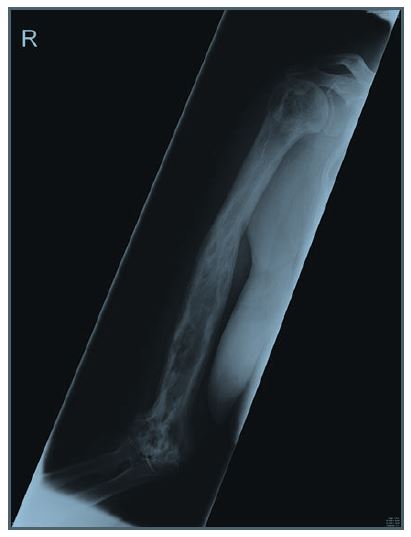
Зачастую у пациентов развивается неврологическая симптоматика из-за деформации позвоночного канала и межпозвонковых отверстий, что вызывает сдавление спинного мозга и спинномозговых нервов. Деформация черепа ведет к сужению отверстий, сдавлению и дислокации головного мозга, потере зрения и слуха, ликвородинамическим расстройствам. Увеличивается риск сердечно-сосудистых заболеваний из-за развития сосудистой кальцификации. Наиболее частые локализации процесса — таз, позвоночник, череп, бедренные и большеберцовые кости. При поражении трубчатых костей измененные кости утолщаются, искривляются, изгиб их иногда сочетается со скручиванием по оси. Костномозговой канал может быть сужен вплоть до облитерации. В позвоночнике процесс локализуется в теле и дуге одного или нескольких, смежных позвонков.
При поражении болезнью Педжета черепа процесс чаще начинается с лобной кости и распространяется на теменную, теменно-височную и затылочную области. Кости лицевого черепа поражаются сравнительно редко. Постепенное увеличение зоны поражения приводит к утолщению, спонгиозированию костей, увеличению величины и формы черепа. Пациент может предъявлять жалобы на то, что его головной убор стал не подходить ему по размеру.
Типичные рентгенологические признаки: остеосклероз с участками остеолиза, увеличение и деформация костей, появление псевдопереломов (лоозеровские зоны на рентгенограмме).
Рекомендуется проведение биопсии, так как возможно развитие редкого осложнения в виде остеосаркомы.
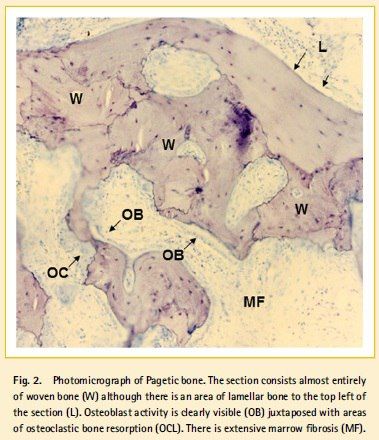
Лечение
Основным показанием для лечения болезни Педжета является появление боли в кости, локализованной на пораженном участке, которая, как полагают, связана с повышенной метаболической активностью. Имеются убедительные доказательства того, что ингибиторы резорбции кости, такие как бисфосфонаты, могут снизить болевой синдром в костях.
В настоящее время нет доказательств в пользу того, что ингибиторы резорбции кости могут предотвратить развитие осложнений болезни Педжета в долгосрочной перспективе, и поэтому лечение чаще носит симптоматический характер.
Вопрос, который долго обсуждался, заключается в том, может ли лечение бифосфонатами благоприятно изменить естественное течение болезни Педжета. Некоторые эксперты считают, что было бы полезно попытаться восстановить нормальный обмен костной ткани в надежде, что это предотвратит осложнения, но пока нет доказательств того, что нормализация костного обмена может предотвратить появление осложнений.
Пациентам со слабой или прерывистой умеренной болью можно назначать НПВС. Если НПВС проявляют низкий анальгетический эффект, то чаще всего анальгетическая терапия используется в качестве дополнения к терапии бисфосфонатом или же только бисфосфонатами.
Бисфосфонаты — это наиболее часто используемые препараты. Они являются структурными аналогами неорганического пирофосфата, которые имеют высокое сродство к связыванию с гидроксиапатитом. Они являются мощными ингибиторами резорбции кости и воздействуют, в основном, на остеокласты, но также оказывают ингибирующее действие на формирование кости.
Азотсодержащие бисфосфонаты (аминобисфосфонаты), такие как памидронат, алендронат, золедронат и ризедронат, в настоящее время являются наиболее широко используемыми для лечения болезни Педжета из-за их большей эффективности. Они ингибируют фарнезилдифосфатную (FPP) синтазу, которая играет центральную роль в мевалонатном пути. Это, в свою очередь, предотвращает пост-трансляционное пренилирование небольших ГТФаз, приводящее к нарушению функции остеокластов.
Существует несколько сравнительных исследований различных аминобисфосфонатов, но те, которые были выполнены, показывают, что золедронат превосходит ризедронат и памидронат в снижении костной массы и улучшении костной боли.
Кальцитонин является ингибитором остеокластов, который, как было установлено, эффективен при улучшении боли в костях и уменьшении биохимических маркеров обмена костной ткани. В настоящее время он редко используется из-за того, что бисфосфонаты удобнее вводить, они дешевле в цене и имеют меньше побочных эффектов.
Деносумаб является ингибитором остеокластов. Это моноклональное антитело, которое нейтрализует RANKL. Это мощный ингибитор резорбции кости. Хотя деносумаб не лицензирован для болезни Педжета, было установлено, что он эффективен в отдельных случаях и может представлять собой вариант лечения, если другие препараты противопоказаны.
Ортопедическая хирургия часто требуется пациентам для фиксации трещин костей, лечения спинального стеноза и для лечения сосуществующего остеоартрита. Клинический опыт показывает, что результат ортопедической хирургии дает хороший эффект, хотя сложность и риск осложнений бывают увеличены из-за деформации и увеличения кровотока через пораженные кости. Бисфосфонаты можно предварительно назначить пациентам для подготовки к операции в надежде, что это предотвратит осложнения, но не ясно, эффективно ли это для снижения риска послеоперационных осложнений.
Многие пациенты нуждаются в повторных курсах лечения. Наиболее распространенной причиной повторного лечения является рецидив боли в костях. По этой причине врачи постоянно контролируют пациентов с болезнью Педжета каждые 6-12 месяцев. Следует отметить, что боль в костях может возникать в результате сопутствующих проблем, таких как остеоартрит, поэтому важна тщательная оценка состояния пациентов, чтобы убедиться, что их боль связана с болезнью Педжета, а не с другой причиной.
Отсутствуют доказательства в пользу того, что профилактический прием бисфосфонатов у пациентов с бессимптомным течением эффективен для предупреждения осложнений.
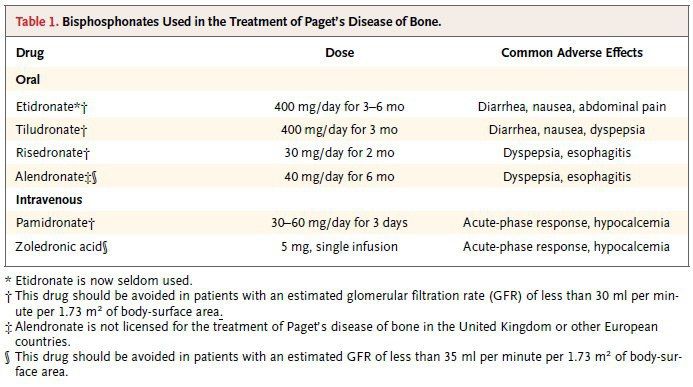
В таблице приведены бисфосфонаты, используемые в настоящее время при лечении. Рандомизированные исследования показали, что аминобисфосфонаты превосходят простые бисфосфонаты, такие как этидронат и тилудронат, в подавлении костного обмена при болезни Педжета. Уровни щелочной фосфатазы начинают падать в течение примерно через 10 дней после начала лечения бисфосфонатом и достигать нормы от 3 до 6 месяцев. Симптомы могут постепенно отступать, в то время как уровни щелочной фосфатазы ещё высоки, но уже начали снижаться (хорошие клинические реакции часто наблюдаются у пациентов, у которых уровень щелочной фосфатазы не восстанавливается до нормы).
Внутривенные бисфосфонаты часто вызывают временную боль в костях, миалгию, головную боль, тошноту, пирексию и усталость в течение 1-3 дней после инфузии (ответ на острую фазу). Эти симптомы могут быть улучшены приемом парацетамола, он вводится до и после инфузии. Но эти симптомы часто исчезают спустя 7 дней после начала лечения.
Наиболее распространенными побочными эффектами являются диспепсия (с ризедронатом и алендронатом) и диарея (с илудронатом и этидронатом). Необычные побочные эффекты бисфосфонатов проявляются увеитом, сыпью и фибрилляцией предсердий; остеонекроз челюсти и атипичные переломы также отмечались как редкие осложнения.
Бисфосфонаты могут вызывать повреждение почек, поэтому противопоказаны пациентам с клинически значимой почечной недостаточностью.
Для борьбы с болью часто используются нефармакологические подходы (акупунктура, физиотерапия, гидротерапия и чрескожная стимуляция электрического нерва), но их эффективность не исследовалась в контролируемых исследованиях. Клинический опыт показывает, что с помощью вспомогательных средств и устройств, таких как трость и обувные лифты, могут быть устранены такие проблемы, как сокращение и деформация конечностей.
Источники
-
Ralston S. H. Paget's disease of bone //New England Journal of Medicine. – 2013. – Т. 368. – №. 7. – С. 644-650.
-
Vallet M., Ralston S. H. Biology and treatment of Paget's disease of bone //Journal of cellular biochemistry. – 2016. – Т. 117. – №. 2. – С. 289-299.
-
Singer F. R. Paget's disease of bone—genetic and environmental factors //Nature Reviews Endocrinology. – 2015. – Т. 11. – №. 11. – С. 662.
-
Нефрология. Ревматология / под ред. Николаса А.Буна, Ники Р. Колледжа, 5) Брайана Р. Уолкера, Джона А.А. Хантера—М.: ООО «Рид Элсивер», 2010
-
Некачалов В.В., Патология костей и суставов. Руководство. — СПб.: Сотис, 2000.
-
David J. et al. Oxford Case Histories in Rheumatology. – Oxford University Press, 2011.